上海六院傅强、张楷乐团队《Adv. Mater.》仿生尿道芯片成功构建!3D 打印 + 仿生微环境,精准模拟尿道瘢痕化,助力药物筛选
01 核心速览
通讯作者及单位
李文尧:上海工程技术大学,材料科学与工程学院
傅强:上海交通大学医学院附属第六人民医院,泌尿外科
张耀鹏:东华大学,材料科学与工程学院,先进纤维材料全国重点实验室
张楷乐:上海交通大学医学院附属第六人民医院,泌尿外科
核心结果
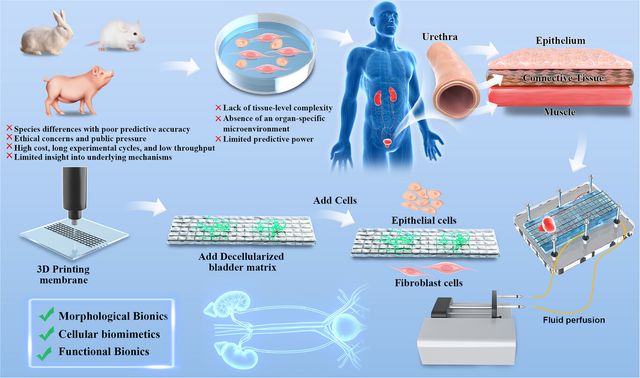
02 研究背景
尿道狭窄是棘手的泌尿系统疾病,核心病理为尿道组织纤维化,导致尿路梗阻,临床复发率高,但没有有效药物。传统研究依赖动物模型(存在物种差异、周期长)和 2D 静态培养(缺乏生理剪切力等关键刺激),难以精准模拟病理微环境。本研究融合微流控、3D 打印与近场静电纺丝技术,构建 BAM 功能化水凝胶微环境的仿生尿道芯片,复现尿道组织的结构与生化复杂性,为纤维化机制研究和药物筛选提供新型体外平台。
03 技术实验
一、尿道芯片的设计与制备
芯片采用“PDMS 外壳 + 复合膜” 结构,通过光固化3D打印制备模具,PDMS按10:1(基底:固化剂)比例浇注,固化后拉伸强度 1800kPa,断裂伸长率 340%,光学透明且弹性良好。复合膜为核心功能组件,结合高温熔融沉积 3D 打印(PCL网格支架)与近场静电纺丝(纳米纤维层),优化后纤维间距0.15mm 时分布最均匀,机械性能优于单一打印方式。
图 1 | 3D 打印器官芯片的制备流程与表征:(A) 展示数字建模、立体光刻 3D 打印与模板浇注的流程;(B) 呈现 3D 打印模具、PDMS 浇注、固化与脱模的过程;(C) 为光固化 3D 打印机制备的模具照片;(D) 展示模具浇注获得的 PDMS 芯片外壳照片;(E) 为设计的 3D 打印芯片模具尺寸示意图;(F) 呈现 PDMS 器官芯片外壳的力学表征结果。 图 2 | 复合 3D 打印膜的工艺优化与机械测试:(A) 展示 3D 打印结合近场静电直写设计制备复合膜的流程;(B) 为不同打印工艺下静电直纺的打印稳定性分布图;(C) 呈现不同打印工艺下静电直纺的实际效果;(D) 展示复合打印与单一打印方式的力学性能对比;(E) 为 96 孔板中明胶(GEL)组和明胶 / BAM(GEL/BAM)组的低倍和高倍观察结果,左下角插图为制备过程中单一明胶(GEL)和复合(GEL/BAM)组的整体外观;(F) 呈现交联到 3D 复合打印膜上的明胶组和 BAM 组的低倍和高倍观察结果(数据以平均值 ± 标准差表示,ns 为无显著差异,p>0.05;*p<0.05;**p<0.01;***p<0.001;*** p<0.0001)。二、BAM 整合与芯片流体模拟
BAM 由兔膀胱组织脱细胞制备,残留 DNA 含量 < 50ng/mg(p<0.0001),与明胶混合后交联到复合膜表面,形成仿生细胞外基质微环境,促进细胞粘附与增殖。通过流体力学模拟优化灌流参数,基于 Navier-Stokes 方程计算,确定 4mm/s 为最优流速,此时芯片内流场均匀,剪切应力符合生理范围(0.2-2dyn/cm²),避免过高压力对细胞造成损伤。
图 3 | 器官芯片的流体模拟建模与分析结果:(A) 展示三组不同流速的速度模拟结果;(B) 为基于流道内设置的 2D 横截面,不同组别的速度变化图;(C) 呈现三组不同流速的压力模拟结果;(D) 展示基于流道内设置的 2D 横截面,不同组别的压力变化图。三、细胞功能与双层共培养验证
芯片微通道经 0.1% 明胶修饰后,PCL 膜接触角从 109.6° 降至 15.8°,PDMS 从 124.3° 降至 36.6°,亲水性显著提升。成纤维细胞(HFF-1)和尿路上皮细胞(SV-HUC-1)在 BAM 功能化膜上增殖活力显著高于明胶组,培养 5 天时活细胞数量明显增多。复合膜的纳米纤维结构可诱导成纤维细胞沿纤维方向定向生长,共聚焦成像证实两种细胞分别在膜的两侧形成双层结构,模拟尿道组织的基质 - 上皮界面。
图 4 | 器官芯片系统的组装过程、气密性测试及添加膀胱脱细胞基质后的生物相容性:(A) 展示 HFF-1 成纤维细胞和 SV-HUC-1 尿路上皮细胞在不同组处理 1、3、5 天后的光密度值;(B) 为加入脱细胞基质后的细胞死活染色测试结果(标尺 = 500μm);(C) 呈现 HFF-1 成纤维细胞在不同组处理 1、3、5 天后的活细胞定量分析结果;(D) 展示 SV-HUC-1 尿路上皮细胞在不同组处理 1、3、5 天后的死活染色图像;(E) 为加入脱细胞基质后的细胞免疫荧光实验结果(标尺 = 200μm);(F) 呈现不同处理组下 SV-HUC-1 尿路上皮细胞 1、3、5 天后 AE1/3 免疫荧光蛋白的相对表达结果;(G) 展示不同处理组下 HFF-1 成纤维细胞 1、3、5 天后 COL1 免疫荧光蛋白的相对表达结果;(H) 呈现不同处理组下 HFF-1 成纤维细胞 1、3、5 天后 α-SMA 免疫荧光蛋白的相对表达结果(数据以平均值 ± 标准差表示,ns 为无显著差异,p>0.05;*p<0.05;**p<0.01;***p<0.001;*** p<0.0001)。 图 5 | 静电流体直写对细胞的影响定量分析及器官芯片中双层细胞空间分布的共聚焦成像:(A) 展示 NC 组、ELC 组和 BAM 组 1、3、5 天后的细胞骨架染色和免疫荧光结果;(B) 为 NC 组成纤维细胞的定向结果;(C) 呈现 BAM 组成纤维细胞的定向结果;(D) 展示 NC 组和 BAM 组成纤维细胞的定向对比;(E) 为共聚焦成像中尿路上皮细胞侧的平面图;(F) 呈现共聚焦成像中静电直写纺丝侧成纤维细胞的平面图;(G) 展示共聚焦成像中双层细胞共培养的 3D 空间分布俯视图;(H) 呈现共聚焦成像中双层细胞共培养的 3D 空间分布正视图。四、纤维化模型构建与药物筛选验证
通过 10ng/mL TGF-β1 诱导纤维化,48 小时后成纤维细胞 α-SMA 荧光强度显著上调(p<0.0001),纤连蛋白 mRNA 和蛋白表达分别增至对照组 3.87 倍和 2.7 倍;尿路上皮细胞 AE1/3 表达下调(p<0.0001),E - 钙粘蛋白降至 0.25 倍,模拟上皮间质转化过程。加入 100nM 雷帕霉素后,成纤维细胞纤维化标志物表达部分抑制,尿路上皮细胞上皮表型部分恢复,证实芯片可用于抗纤维化药物的效果评估。
图 6 | 不同对比组的差异表达基因(DEGs)及功能富集分析:(A) 展示 F_BAM 与 F_ELC、F_STA 与 F_SHR、S_STA 与 S_SHR 三个关键对比组的差异表达基因对比热图;(B) 为与纤维化相关的差异表达基因;(C) 呈现 S_STA 与 S_SHR 对比组差异表达基因的 GO 功能富集分析;(D) 展示 S_STA 与 S_SHR 对比组差异表达基因的 KEGG 通路富集分析;(E) 为 F_STA 与 F_SHR 对比组差异表达基因的 GO 功能富集分析;(F) 呈现 F_STA 与 F_SHR 对比组差异表达基因的 KEGG 通路富集分析;(G) 展示 S_STA 与 S_SHR 对比组差异表达基因的 GO 功能富集分析;(H) 呈现 S_STA 与 S_SHR 对比组差异表达基因的 KEGG 通路富集分析。 图 7 | 细胞增殖相关分子机制和信号通路的整合分析:(A、B) 展示 S_STA 与 S_SHR 对比组中与细胞增殖相关的前 20 个上调(A)和下调(B)基因的热图;(C) 为 S_STA 与 S_SHR 对比组中与细胞增殖相关的差异表达基因构建的蛋白质 - 蛋白质相互作用网络;(D-F) 呈现 F_BAM 与 F_ELC 对比组中显著富集的信号通路,包括 JAK-STAT 信号通路(D)、IL-17 信号通路(E)和 PPAR 信号通路(F)。 图 8 | 不同干预条件下两种细胞的 CCK-8 分析、免疫荧光表达分析、PCR 和 Western blot 检测药物效果:(A) 展示各处理组成纤维细胞在第 2 天和第 4 天的 α-SMA 免疫荧光图像;(B) 为各处理组第 2 天和第 4 天 α-SMA 的相对表达对比;(C) 呈现各处理组尿路上皮细胞在第 2 天和第 4 天的 AE1/3 免疫荧光图像;(D) 展示各处理组第 2 天和第 4 天 AE1/3 的相对表达对比;(E) 为各处理组下成纤维细胞中纤连蛋白的相对 mRNA 表达;(F) 呈现各处理组下尿路上皮细胞中 E - 钙粘蛋白和 AE1 的相对 mRNA 表达;(G) 展示 HFF-1 细胞的 Western blot 结果;(H) 呈现 SV-HUC-1 细胞的 Western blot 结果;(I) 为各处理组下成纤维细胞中纤连蛋白的相对蛋白表达;(J) 呈现各处理组下尿路上皮细胞中 E - 钙粘蛋白和 AE1 的相对蛋白表达(数据以平均值 ± 标准差表示,ns 为无显著差异,p>0.05;*p<0.05;**p<0.01;***p<0.001;*** p<0.0001)。04 结论与展望
本研究成功构建了仿生尿道芯片平台,通过 3D 打印、近场静电纺丝与 BAM - 明胶水凝胶功能化,复现了尿道组织的结构特征与生理微环境。该芯片可精准模拟尿道纤维化的核心病理过程(成纤维细胞激活、上皮间质转化),且能有效评估抗纤维化药物(如雷帕霉素)的干预效果,为尿道狭窄的机制研究和药物筛选提供了新型体外工具。
未来可进一步优化芯片结构,构建圆形管腔模拟真实尿道形态,整合免疫细胞、血管内皮细胞等成分提升模型复杂性;结合患者来源的细胞或类器官,开发个性化尿道芯片平台,为精准医疗和再生医学提供更有力的支持。
05 原文信息










